近日,我院王琳辉副教授课题组在神经退行性疾病领域权威期刊《npj Parkinson's Disease》(中科院一区Top期刊,五年平均影响因子:8.3)在线发表题为“Perivascular spread of CSF-derived α-synuclein oligomers drives region-specific Parkinson's-like pathology”的研究论文,首次系统阐明脑脊液中的α-突触核蛋白寡聚体(α-SOs)经血管周围间隙(perivascular spaces, PVSs)扩播入脑是促进帕金森病(Parkinson's Disease,PD)脑内区域特异性病理损伤的关键机制,为PD早期干预与治疗提供全新理论依据与靶向策略。

帕金森病(PD)是一种常见神经退行性疾病,其核心病理为黑质(SN)多巴胺能(DA)神经元退变和α-突触核蛋白(α-syn)异常聚集。值得注意的是,PD不仅表现为运动功能障碍,其嗅觉障碍等非运动症状常早于运动症状出现。大量研究证实α-SOs具有较强的神经毒性,临床研究发现PD患者脑脊液中α-SOs水平显著升高,那么脑脊液中的α-SOs能否重新进入脑组织从而驱动PD特异性病理进展呢?这是长期以来该领域亟待破解的一个关键科学问题。
该课题组利用组织透明化3D成像、荧光显微光学切片断层成像(fMOST)、免疫荧光和分子生物学等技术,直观证实脑脊液来源的α-SOs并非通过突触传递,而是经PVSs扩散进入脑实质,且在脑内呈现显著脑区特异性--嗅球(OB)摄取量远高于黑质(SN)。这一发现打破既往 “α-SOs仅沿神经环路突触传播” 的传统认知,首次指出PVSs是PD病灶扩播的重要非突触通路。
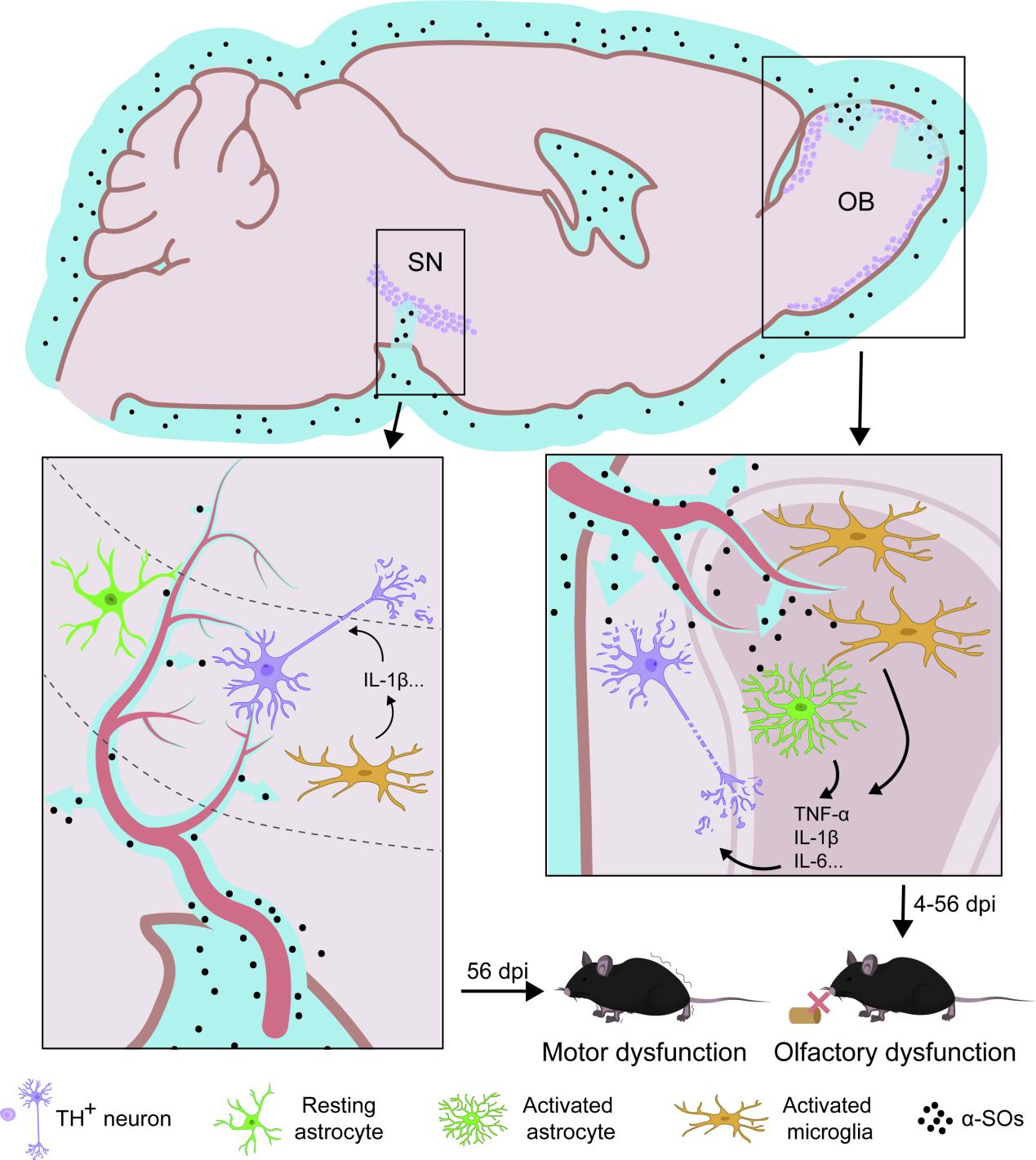
该团队通过向小鼠侧脑室注射α-SOs构建动物模型,完整还原PD “先嗅觉障碍、后运动障碍” 的典型病程(见下图)。研究发现,富集于嗅球的α-SOs会快速激活小胶质细胞与星形胶质细胞,显著上调TNF-α、IL-6、IL-1β等促炎因子表达,引发强烈的局部神经炎症反应,进而导致嗅球内DA神经元发生急性且长期持续性的退行性丢失,直接诱发早发性且持久的嗅觉功能障碍;而黑质区域因脑脊液流入量少,α-SOs摄取与炎症反应均较弱,仅在病理进展后期出现DA神经元损伤,最终表现为迟发性的运动功能障碍。进一步研究发现,OB的特异性病理损伤和嗅觉功能损伤的程度与α-SOs的注射剂量呈现显著的依赖性。
该研究不仅扩展了人们对PD发病机制的认识,更为临床提供了可转化的干预方向,提示清除脑脊液中的致病性α-SOs能够有效减轻脑内神经炎症与神经元损伤,为PD的早期预警、靶向治疗以及病程延缓提供了全新理论依据与策略参考。该研究同时对路易体痴呆(dementia with Lewy bodies)、多系统萎缩(multiple system atrophy)等其他突触核蛋白病(synucleinopathies)的机制研究与干预探索也具有重要的借鉴价值。
该研究以苏州大学苏州医学院基础医学院为第一完成单位,硕士研究生朱温欣为第一作者,王琳辉副教授为唯一通讯作者。本研究得到了国家自然科学基金委员会的资助。据悉,王琳辉课题组近年来聚焦研究水孔蛋白4(AQP4)介导的胶质淋巴系统(glymphatic system)在帕金森病和慢性应激中的变化和作用,相关成果相继发表在J Cereb Blood Flow Metab、Mol Neurobiol、CNS Neurosci Ther、Neurosci Bull、Psychopharmacology等国际学术期刊。此次在《npj Parkinson's Disease》发表的文章是该团队基于多年潜心研究取得的又一突破性进展。
原文链接:https://www.nature.com/articles/s41531-026-01300-3

