近日,我院李明辉教授课题组在PNAS上发表题为《An interpretable molecular framework for predicting cancer driver missense mutations》的研究论文。该研究围绕癌症基因组学中的核心难题—如何从海量错义突变中精准识别真正驱动肿瘤发生发展的关键突变,提出了一种兼具预测性能与分子机制可解释性的计算框架MutaPheno。论文以苏州大学为第一完成单位发表,硕士研究生杨艳为第一作者,李明辉教授为通讯作者。

在肿瘤基因组中,每个肿瘤通常携带成千上万个基因突变,但其中真正对肿瘤发生和进展起决定性作用的驱动突变仅占极少数。受限于癌症驱动突变标注稀缺、突变功能机制复杂等因素,现有预测方法在准确性和可解释性方面仍面临挑战。针对上述问题,研究团队系统整合并分析了超过12万个 来自不同生物学语境的错义突变,从蛋白结构稳定性、功能位点分布、蛋白互作界面及生物物理扰动等多个层面,全面刻画了驱有害突变与中性突变之间的分子表型差异。
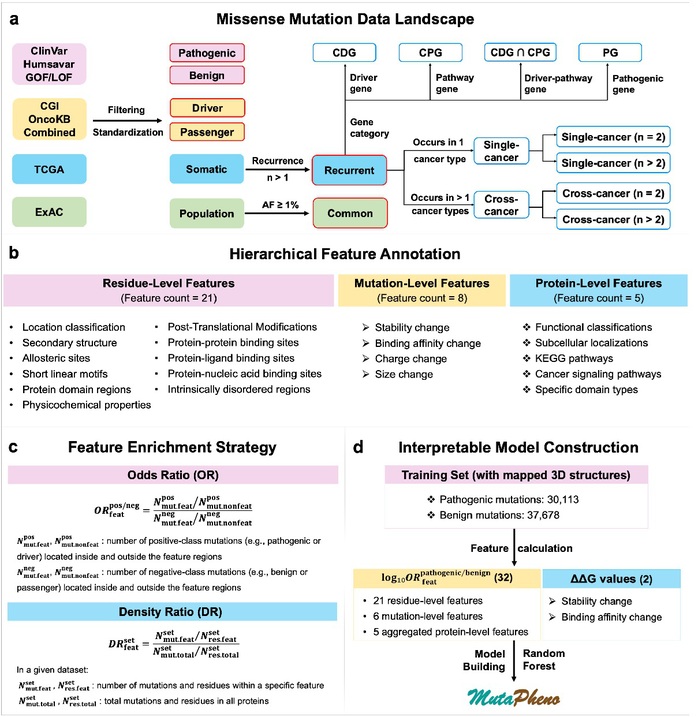
在此基础上,团队构建了可解释的预测模型MutaPheno。该模型整合34项具有明确生物学含义的分子特征,仅使用遗传病致病/良性突变进行训练,即可在癌症突变场景中准确识别驱动突变,并在未见蛋白和跨数据集测试中表现出良好的泛化能力和概率校准性能。研究结果表明,遗传病致病突变与癌症驱动突变在分子机制层面具有显著共性,为利用可迁移的机制证据缓解癌症突变标注稀缺问题提供了新的研究思路。
该研究为癌症关键突变筛选、潜在治疗靶点发现以及精准医学研究提供了具有可解释性和可推广性的计算方法。
本研究得到了国家自然科学基金面上项目资助。
原文链接:https://www.pnas.org/doi/full/10.1073/pnas.2524289123

